 , характеризующее зависимость осмотического давления от концентрации и температуры, применимо …
, характеризующее зависимость осмотического давления от концентрации и температуры, применимо …
Для разбавленных растворов сильных и слабых электролитов в уравнение закона Вант-Гоффа 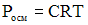 вводится изотонический коэффициент, зависящий от степени диссоциации электролита и числа ионов, образующихся при его диссоциации.
вводится изотонический коэффициент, зависящий от степени диссоциации электролита и числа ионов, образующихся при его диссоциации.
Уравнение закона Вант-Гоффа 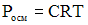 в данном виде применимо только к разбавленным растворам неэлектролитов. Для разбавленных растворов электролитов вводится изотонический коэффициент, зависящий от степени диссоциации электролита и числа ионов, образующихся при его диссоциации. Для концентрированных растворов уравнение дает неверные результаты.
в данном виде применимо только к разбавленным растворам неэлектролитов. Для разбавленных растворов электролитов вводится изотонический коэффициент, зависящий от степени диссоциации электролита и числа ионов, образующихся при его диссоциации. Для концентрированных растворов уравнение дает неверные результаты.
Для разбавленных растворов электролитов в уравнение закона Вант-Гоффа 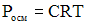 вводится изотонический коэффициент, зависящий от степени диссоциации электролита и числа ионов, образующихся при его диссоциации.
вводится изотонический коэффициент, зависящий от степени диссоциации электролита и числа ионов, образующихся при его диссоциации.